
Del Gen al Metaboloma: Un Viaje Audaz a la Salud de Precisión a Través de la Visión Multiómica
9 de julio de 2025
Análisis Clínico del Propionato de Imidazol (ImP): Nuevo Biomarcador de Aterosclerosis. Aplicabilidad Clínica Inmediata
22 de julio de 2025
Resumen
El edema funcional leve a moderado, particularmente en contextos de origen vascular, hormonal o ambiental, constituye un desafío terapéutico frecuente en la práctica clínica. Frente a las limitaciones de los diuréticos convencionales —como la desmineralización, la activación compensatoria del sistema renina-angiotensina-aldosterona (RAAS) y la baja tolerancia a largo plazo—, la fitoterapia racional ofrece un abordaje más fisiológico, seguro y multidimensional. Esta revisión analiza la evidencia experimental, clínica y etnofarmacológica disponible sobre extractos vegetales con acción antiedematosa, agrupados por mecanismo principal. Se destacan especies con efecto diurético tubular directo, como Equisetum arvense y Petroselinum crispum; moduladores del RAAS ricos en potasio como el citrato y gluconato potásico; y agentes con actividad venotónica, antioxidante o antiinflamatoria, entre ellos Crataegus monogyna, Camellia sinensis y Filipendula ulmaria. Asimismo, se revisan plantas con acción drenante y antiséptica urinaria, como Zea mays, Arctostaphylos uva-ursi, Agathosma betulina y Vaccinium macrocarpon, útiles en pacientes con riesgo de infecciones urinarias recurrentes. En conjunto, los datos disponibles respaldan el uso de combinaciones fitoterapéuticas estandarizadas como una herramienta eficaz y bien tolerada para el manejo del edema no complicado, especialmente en poblaciones sensibles o escenarios de uso prolongado.
Introducción
El edema constituye una manifestación clínica caracterizada por el incremento anormal del volumen del líquido intersticial en los tejidos corporales, resultado de un desbalance entre los mecanismos que regulan el intercambio de fluidos a nivel capilar y linfático. [1,2] Esta alteración no responde a un fenómeno único, sino a una convergencia multifactorial de disfunciones hemodinámicas, oncóticas, inflamatorias, osmóticas y neurohormonales. [1,3] Tales mecanismos interactúan de forma dinámica, modulando el equilibrio hidroeléctrico entre el compartimento intravascular y el espacio extravascular. [2,4] Desde el punto de vista clínico, el edema no debe entenderse únicamente como un signo inespecífico, sino como una manifestación integradora que refleja disfunciones en diferentes sistemas reguladores del volumen extracelular. [1,3] En este contexto, la fitoterapia, particularmente cuando se basa en fórmulas racionales, estandarizadas y bien toleradas, puede contribuir como una herramienta terapéutica de gran utilidad. [4] Especialmente relevantes aquellas combinaciones botánicas que inducen una diuresis fisiológica sin provocar desmineralización, deshidratación ni alteraciones del equilibrio electrolítico, permitiendo un abordaje sintomático seguro y sostenible del edema leve a moderado en la práctica clínica. [5]
Fisiopatología
La génesis del edema se comprende mejor a partir de los principios de la ecuación modificada de Starling, que describe la distribución de líquidos entre el comportamiento intravascular y el espacio intersticial como resultado del balance entre la presión hidrostática capilar, la presión oncótica plasmática, la permeabilidad endotelial y el drenaje linfático. [2] Cualquier disrupción en estos determinantes, aislada o combinada, puede favorecer el desplazamiento neto de fluido hacia el intersticio, dando lugar a acumulación tisular progresiva. [2,3]
Entre los principales mecanismos fisiopatológicos implicados destacan:
- Incremento de la presión capilar hidrostática, observando frecuentemente en situaciones de sobrecarga circulatoria como la insuficiencia cardiaca congestiva, la insuficiencia venosa crónica o la obstrucción del retorno venoso o linfático. Esta elevación promueve la salida forzada de fluido desde los capilares hacia los tejidos [2].
- Reducción de la presión oncótica plasmática, secundaria a hipoalbuminemia, hipoproteinemia o pérdidas proteicas excesivas (como ocurre en el síndrome nefrótico, enteropatías perdedoras de proteínas o desnutrición grave). Al disminuir la fuerza de retención intravascular, se favorece el escape de líquido hacia el intersticio [3].
- Aumento de la permeabilidad capilar, característico de procesos inflamatorios agudos o crónicos, reacciones inmunoalérgicas o daño endotelial directo, que permite la extravasación de proteínas plasmáticas y líquido, exacerbando el edema.
- Activación de sistemas neurohormonales, especialmente el sistema renina-angiotensina-aldosterona (RAAS) y la hormona antidiurética (ADH), que inducen retención renal de sodio y agua, perpetuando el aumento del volumen extracelular y contribuyendo al mantenimiento del estado edematoso [2,4].
- Factores predisponentes funcionales o ambientales, como el sedentarismo, la ingesta elevada de sodio, las variaciones hormonales (síndrome premenstrual, embarazo), la exposición a altas temperaturas o el uso de determinados fármacos (antiinflamatorios, calcioantagonistas), pueden actuar como catalizadores de la formación edematosa, incluso en ausencia de enfermedad estructural primaria [2,3,6].
Este fenómeno, aunque inicialmente puede cursar de forma subclínica, tiende a manifestarse progresivamente con signos y síntomas como tumefacción, pesadez o tensión cutánea, reducción de la movilidad articular, y, en algunos casos con mayor riesgo de complicaciones como celulitis, ulceraciones o trombosis venosa profunda [2].
Fundamentos experimentales y clínicos de los agentes fitoterapéuticos con acción antiedematosa
El desarrollo de estrategias terapéuticas basadas en fitoterapia ha adquirido progresiva relevancia en el abordaje de condiciones clínicas de curso crónico o funcional, como el edema leve o moderado. Desde una perspectiva basada en la evidencia, diversas especies vegetales han sido estudiadas por su capacidad para modular las vías fisiopatológicas implicadas en la génesis y mantenimiento del edema; alteraciones hemodinámicas, disfunción endotelial, hiperactivación neurohormonal y sobrecarga tisular. [5]
A diferencia de los diuréticos sintéticos, muchos compuestos botánicos muestran un perfil de acción más fisiológico, promoviendo una diuresis efectiva sin generar depleción significativa de electrolitos ni comprometer la perfusión renal. [5,7] Esta propiedad es particularmente relevante en contextos clínicos donde el uso prolongado de fármacos depletores puede asociarse a efectos adversos, disminución de la adherencia terapéutica y deterioro de la calidad de vida.
El respaldo a su uso se encuentra distribuido en distintos niveles de evidencia, que abarcan desde la investigación etnobotánica hasta ensayos clínicos aleatorizados, pasando por estudios de farmacodinámica renal en modelos animales y humanos. [5,7] La relevancia terapéutica de estos compuestos depende tanto de su composición fitoquímica como de su estandarización galénica, dosis efectiva y vía de administración. A este respecto, algunos principios activos destacan especialmente por su reproducibilidad farmacológica, tolerancia clínica y efecto sinérgico cuando se combinan con otros agentes de acción complementaria. [3,6]
Agentes fitoterapéuticos con efecto diurético tubular directo
El aumento controlado de la diuresis representa uno de los pilares fundamentales en el tratamiento sintomático del edema. En el ámbito fitoterapéutico, ciertas especies vegetales han demostrado capacidad para inducir una excreción urinaria efectiva mediante la modulación de los mecanismos renales de reabsorción tubular de agua y electrolitos, actuando de forma análoga, aunque generalmente más suave, a los diuréticos sintéticos. [5,7] A diferencia de estos últimos, cuyo efecto abrupto y a menudo desmineralizante puede comprometer la homeostasis iónica y la función renal, los agentes botánicos con actividad tubular directa parecen ofrecer un perfil farmacodinámico más progresivo, sostenido y fisiológico. [7,8]
Entre los fitocomponentes con evidencia más robusta se encuentra Equisetum arvense (cola de caballo), planta tradicionalmente utilizada con fines diuréticos, pero cuyo efecto ha sido validado además por ensayos clínicos modernos. [7] Un estudio aleatorizado, doble ciego, con diseño cruzado, demostró unos resultados en la excreción urinaria comparable a la del agente tiazídico, pero sin alteraciones en la eliminación de sodio o potasio ni alteraciones en parámetros bioquímicos hepatorrenales, lo que sugiere una eficacia diurética clínicamente relevante con un excelente perfil de seguridad. Estos efectos se atribuyen a la acción conjunta de flavonoides, derivados fenólicos, potasio y sílice presentes en su composición fitoquímica. [5,7]
Otro ejemplo es Petroselinum crispum (perejil), del cual se han descrito efectos natriuréticos y acuoréticos consistentes en estudios preclínicos. En modelos de perfusión renal y experimentación in vivo, el extracto acuoso de semillas demostró inhibir la actividad de la bomba Na⁺/K⁺-ATPasa en las células del túbulo renal, reduciendo la reabsorción activa de sodio y provocando un arrastre osmótico de agua. Este efecto fue dependiente de la presencia de potasio en el lumen tubular y se mantuvo incluso en condiciones de hiponatremia experimental, sugiriendo un mecanismo selectivo y adaptable. Además, se ha evidenciado su acción antioxidante renal y su potencial efecto protector frente al daño tubular inducido por nefrotóxicos.[7]
Otras especies como Betula pendula (abedul), Orthosiphon aristatus (ortosifón) y Urtica dioica (ortiga mayor) han sido tradicionalmente utilizadas con fines diuréticos y muestran actividad comparable en estudios preclínicos. Aunque la evidencia clínica controlada para estas plantas es más limitada, su inclusión en complejos fitoterapéuticos se apoya en la coherencia de sus mecanismos fisiológicos y en una larga trayectoria de uso etnofarmacológico. [5,9]
Desde un punto de vista comparativo, los extractos vegetales con acción tubular directa no igualan en potencia a los diuréticos de asa, pero presentan una ventaja importante: inducen una movilización de agua libre y sodio sin producir alteraciones significativas en la kaliemia ni en la perfusión renal. Esto resulta especialmente útil en pacientes con edema de origen funcional, en quienes se prioriza una intervención sostenida y bien tolerada por encima de una eliminación aguda de volumen. [5,7]
En resumen, las plantas con capacidad diurética tubular directa, en particular Equisetum arvense y Petroselinum crispum, presentan evidencia experimental y clínica que respalda su eficacia como agentes antiedematosos suaves, seguros y compatibles con la fisiología renal. Su acción se potencia cuando se emplean dentro de combinaciones racionales y estandarizadas, diseñadas para cubrir múltiples dianas fisiopatológicas del edema sin comprometer el equilibrio homeostático del paciente. [6,7]
Moduladores del RAAS
Uno de los desafíos más relevantes en el manejo terapéutico del edema es evitar los mecanismos de retroalimentación compensatoria que reducen la eficacia de los tratamientos diuréticos y agravan el estado hidrosalino del paciente. [5] En este contexto, la activación del RAA desempeña un papel central. La disminución del volumen plasmático efectivo inducida por la diuresis, ya sea farmacológica o fisiológica, suele desencadenar una respuesta compensatoria en el aparato yuxtaglomerular, que secreta renina y desencadena una cascada hormonal destinada a conservar sodio y agua a través de la aldosterona y la vasopresina. Este fenómeno, si no se modula adecuadamente, puede conducir a una retención secundaria de líquidos, limitando la eficacia del abordaje diurético y perpetuando el cuadro edematoso. [5,7,10,11][Imagen 1]
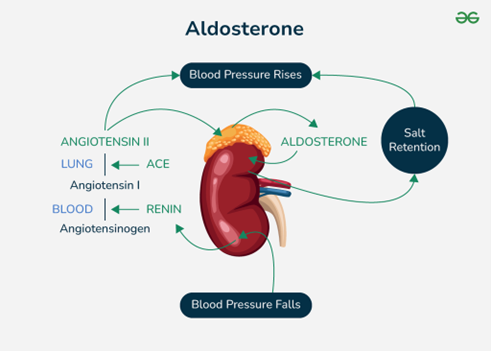
Imagen 1: Activación del sistema RAAS y su efecto sobre la presión arterial y la retención de sodio.
Desde la perspectiva fitoterapéutica, algunos principios activos de origen vegetal han demostrado capacidad para interferir de forma directa o indirecta con esta vía hormonal, contribuyendo así a mantener la eficacia del tratamiento y a evitar la sobrecarga iónica compensatoria. Un enfoque especialmente interesante se basa en el uso de agentes ricos en potasio, como el gluconato y el citrato potásico, presentes de forma natural en algunas especies vegetales y empleados también como suplementos bioactivos. El potasio ejerce un efecto inhibidor fisiológico sobre la secreción de aldosterona a nivel de la zona glomerulosa de la corteza suprarrenal, efecto demostrado en múltiples modelos experimentales y reconocido en fisiología clínica. Al reducir la concentración de aldosterona circulante, se atenúa la reabsorción distal de sodio y se favorece una diuresis sostenida sin efectos de rebote. [9,12,13](Imagen 2)
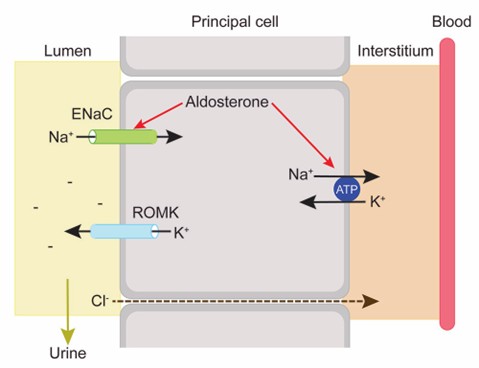
Imagen 2: Influencia del potasio en la secreción de aldosterona y su efecto sobre el transporte iónico renal.
Esta modulación del RAAS también ha sido sugerida para ciertos compuestos flavonoides y triterpenoides presentes en extractos de Equisetum arvense y Petroselinum crispum. [6,7,12] Aunque los datos clínicos directos en humanos son aún escasos, estudios en animales y modelos celulares han reportado una disminución en la expresión génica de componentes del sistema RAAS, incluyendo receptores AT1 y la propia enzima convertidora de angiotensina (ECA), así como una reducción en los niveles de aldosterona urinaria tras la administración repetida de algunos de estos extractos. Estas observaciones, aunque preliminares, apuntan hacia un posible efecto antialdosterónico indirecto que podría reforzar la acción diurética sin provocar activación refleja del eje hormonal. [12]
Adicionalmente, ciertos compuestos vegetales —incluyendo los presentes en Orthosiphon aristatus y Urtica dioica— contienen minerales, ácidos fenólicos y flavonoides que contribuyen a regular la presión arterial y mejorar la perfusión renal, dos factores estrechamente vinculados con la activación del sistema renina–angiotensina. [5,8] Si bien el nivel de evidencia clínica para estos efectos es más limitado, su inclusión en formulaciones racionales se sustenta en mecanismos plausibles y en observaciones empíricas consistentes.
Cabe destacar que, a diferencia de los antagonistas farmacológicos directos del RAAS (como los IECA, ARA II o antialdosterónicos), los moduladores fitoterápicos no bloquean completamente la respuesta hormonal, sino que la ajustan a un nivel más fisiológico, reduciendo así el riesgo de efectos secundarios como hiperpotasemia, hipotensión sintomática o deterioro agudo de la función renal. Esto los convierte en herramientas especialmente útiles en pacientes con edema funcional o en fases iniciales de retención de líquidos, donde el objetivo es restaurar el equilibrio hidrosalino sin inducir compensaciones deletéreas. [9,12]
En conjunto, la evidencia disponible respalda el uso de ciertos compuestos fitoterapéuticos como moduladores suaves del eje RAAS, capaces de favorecer una respuesta diurética sostenida y fisiológica. [5-7] Su inclusión en programas terapéuticos orientados al manejo del edema representa una estrategia racional, segura y complementaria a otros mecanismos de acción. [9,12]
Estabilizadores de la permeabilidad capilar y agentes antiinflamatorios
Además de los factores hemodinámicos y hormonales, la disrupción de la barrera endotelial capilar constituye un mecanismo central en la fisiopatología del edema, especialmente en contextos inflamatorios, alérgicos o inmunomediados. La activación de citoquinas proinflamatorias (como TNF-α, IL-1β e IL-6), la liberación de radicales libres de oxígeno y la alteración de las proteínas de unión intercelular, incluidas ocludinas y claudinas, aumentan la permeabilidad vascular, favoreciendo la extravasación de fluido plasmático hacia el espacio intersticial. Este tipo de edema, de origen inflamatorio o neurovascular, responde mal a los diuréticos convencionales, y requiere una intervención dirigida a modular la respuesta inflamatoria y estabilizar la integridad endotelial. [5,14,15]
En este contexto, diversos agentes fitoterapéuticos han demostrado efectos antiinflamatorios, antioxidantes y vasoprotectores que contribuyen a restaurar la funcionalidad de la barrera vascular y reducir la formación de edema. Entre ellos, destacan por su solidez científica los extractos de Filipendula ulmaria (reina de los prados), Crataegus monogyna (espino albar) y Camellia sinensis (té verde). [9,14]
El extracto de Filipendula ulmaria contiene derivados salicílicos naturales, taninos y flavonoides que ejercen una actividad antiinflamatoria leve a moderada. En modelos animales y estudios in vitro, se ha observado una reducción significativa en la producción de prostaglandinas proinflamatorias y una atenuación de la respuesta leucocitaria local, lo cual contribuye a preservar la integridad de la pared capilar. Esta acción estabilizadora resulta especialmente útil en edemas con componente alérgico o congestivo. [5]
Crataegus monogyna, por su parte, ha sido ampliamente estudiado por su actividad vasoprotectora. Los flavonoides presentes en sus hojas y flores, como la vitexina y la hiperósida, han demostrado capacidad para mejorar la contractilidad de la musculatura vascular lisa, aumentar la resistencia capilar y reducir la permeabilidad inducida por histamina y otras aminas vasoactivas. [9,14,16] Estas propiedades lo convierten en un agente de elección en el manejo de edemas secundarios a insuficiencia venosa crónica o fragilidad vascular. [8,9].
Un papel destacado merece también Camellia sinensis, planta rica en catequinas (en particular epigalocatequina-3-galato, EGCG), con potente acción antioxidante y antiinflamatoria. Diversos estudios han documentado su capacidad para inhibir la activación del factor de transcripción NF-κB, reducir la generación de especies reactivas de oxígeno (ROS) y preservar la arquitectura de la barrera endotelial en modelos de daño vascular inducido. [17-19] Además, sus efectos positivos sobre la presión arterial y la función endotelial le confieren un perfil beneficioso adicional en situaciones donde el componente hemodinámico y el inflamatorio coexisten, como ocurre en el edema mixto de origen venoso-inflamatorio. [19-21]
Otros compuestos, como Urtica dioica (ortiga mayor), poseen también propiedades inmunomoduladoras que podrían contribuir a la reducción de la respuesta inflamatoria sistémica, si bien la evidencia clínica en relación específica al edema es más limitada. [22]
Cabe subrayar que la acción de estos agentes no se limita a la simple reducción del edema visible, sino que se orienta a preservar la función de la barrera microvascular, regulando tanto la estructura como la función del endotelio y evitando el paso incontrolado de componentes plasmáticos al intersticio. Este abordaje es complementario al efecto diurético, y esencial en cuadros donde el edema no responde exclusivamente a cambios en el volumen intravascular. [8,10]
En conjunto, los agentes fitoterapéuticos con propiedades antiinflamatorias y estabilizadoras capilares aportan un mecanismo terapéutico diferencial y clínicamente relevante. Su incorporación en estrategias antiedematosas resulta especialmente indicada cuando existe un componente inflamatorio vascular, como en los edemas dependientes, el edema premenstrual o aquellos asociados a disfunción microcirculatoria crónica. [5,8,10]
Agentes venotónicos y linfocinéticos
El componente hemodinámico del edema no se limita al aumento de la presión hidrostática arterial; en muchos casos, especialmente en las extremidades inferiores, intervienen fenómenos de insuficiencia venosa crónica, estasis microvascular y disfunción del drenaje linfático, todos los cuales contribuyen de manera significativa a la acumulación de líquido intersticial. [5,8,19] La reducción de la velocidad del flujo venoso, la dilatación de los vasos capacitantes y el fallo en las válvulas venosas favorecen la extravasación plasmática prolongada, lo cual se traduce clínicamente en edemas de instauración lenta, con fóvea positiva, peor en bipedestación y con escasa respuesta a diuréticos aislados. [8]
En este tipo de edema, el abordaje debe incluir la mejora de la función venosa y el estímulo del retorno linfático. Algunas plantas medicinales presentan efectos venotónicos y linfocinéticos, actuando sobre el tono de la pared vascular, la permeabilidad capilar y la viscosidad sanguínea. Estas acciones son complementarias e incluso fundamentales en el tratamiento del edema de origen vascular. [5,8]
Uno de los fitocomponentes más estudiados en este ámbito es Crataegus monogyna (espino albar). Además de sus propiedades vasodilatadoras moderadas sobre el árbol arterial coronario y cerebral, esta especie ha demostrado mejorar el tono venoso a través de la estimulación del músculo liso vascular, con incremento de la contractilidad de las paredes venulares y reducción del volumen de estasis. [8,9,19] Los flavonoides de Crataegus, particularmente la vitexina, refuerzan la resistencia capilar y disminuyen la fragilidad vascular, efectos útiles en pacientes con tendencia a la extravasación o hematomas espontáneos. [20]
Otra especie relevante es Juniperus communis (enebro), tradicionalmente utilizada por su efecto diurético, pero que además posee una leve acción vasomoduladora mediada por monoterpenos (α-pineno, mirceno), los cuales inducen una vasodilatación suave con mejora del retorno venoso. En estudios preclínicos se ha observado también un potencial efecto estimulante sobre el drenaje linfático, aunque este mecanismo aún no ha sido completamente elucidado en humanos. [5]
De forma complementaria, diversas plantas con efecto antioxidante y antiinflamatorio, como Camellia sinensis, Filipendula ulmaria y Urtica dioica, contribuyen a reducir el edema dependiente al mejorar la reactividad vascular y limitar el daño endotelial inducido por el estrés oxidativo, lo que preserva la función del sistema de válvulas venosas y mantiene el flujo laminar efectivo. [10,11,14,22]
Aunque la linfocinesis no es fácilmente medible en modelos clínicos humanos, se ha propuesto que algunas sustancias naturales estimulan indirectamente la contractilidad de los vasos linfáticos, facilitan el vaciamiento ganglionar o mejoran la absorción de proteínas plasmáticas intersticiales, lo que reduciría la presión oncótica tisular y favorecería la reabsorción de fluido. [5] Si bien la evidencia directa aún es incipiente, se considera plausible que el efecto venotónico y linfocinético actúe de forma integrada en estas formulaciones.
Este grupo de fitocompuestos, por tanto, desempeña un papel crucial en el tratamiento del edema crónico de origen vascular o mixto, en especial cuando la intervención se realiza de forma preventiva, sostenida y combinada con medidas no farmacológicas como el ejercicio, el drenaje manual o el uso de medias de compresión. [14,22]
Desde el punto de vista clínico, su uso permite reducir la dependencia de diuréticos, mejorar la sensación de pesadez y evitar el círculo vicioso de estasis-inflamación-hipoperfusión, que caracteriza al edema crónico mal tratado. Por esta razón, su integración en esquemas terapéuticos para el manejo de la retención de líquidos de origen periférico está cada vez más respaldada por consensos de expertos en fitoterapia y microangiopatía funcional. [5,8,19]
Cofactores depurativos, drenantes urinarios y preventivos de infección del tracto urinario
Además de los mecanismos clásicos que inducen y perpetúan el edema, existen factores metabólicos y urológicos que pueden interferir con el manejo clínico del líquido intersticial, especialmente cuando se trata de edemas funcionales, crónicos o de baja respuesta farmacológica. [5] En este contexto, los agentes fitoterapéuticos con capacidad para estimular el drenaje urinario fisiológico, favorecer la eliminación de metabolitos nitrogenados y prevenir procesos infecciosos uropáticos representan una herramienta valiosa para optimizar el tratamiento y prevenir complicaciones. [5,23,24]
Entre los cofactores vegetales de mayor interés destaca Zea mays (seda de maíz), tradicionalmente empleada por su efecto diurético suave, mediado por saponinas, flavonoides y sales minerales. Su acción osmótica, junto con una ligera irritación tubular benigna, incrementa el volumen urinario sin provocar deshidratación significativa ni alterar la concentración plasmática de electrolitos. [12,23] Además, su contenido en potasio favorece el perfil iónico global del tratamiento. Aunque carece de ensayos clínicos a gran escala, los datos preclínicos y su uso tradicional respaldan su inclusión en protocolos dirigidos a la movilización progresiva de líquidos retenidos. [4,5,13]
Arctostaphylos uva-ursi (gayuba) y Agathosma betulina (buchú) presentan una doble acción que las hace particularmente útiles en este contexto. Por un lado, contienen arbutina, un glucósido fenólico que se transforma en hidroquinona en el tracto urinario y actúa como antiséptico urotelial. [24] Por otro, ambas plantas poseen efectos diuréticos suaves, lo que permite aumentar la frecuencia miccional y reducir la concentración bacteriana en la vejiga. Esta actividad es relevante en pacientes con edemas recurrentes y tendencia a infecciones del tracto urinario inferior, en quienes el estancamiento de orina por reducción del flujo o vaciado incompleto constituye un factor de riesgo. [1,3, 24] La evidencia preclínica y observacional sugiere una eficacia preventiva en ITU de repetición, particularmente cuando se emplean de forma sostenida y en conjunto con otros componentes bioactivos. [2,25,26] (Imagen 3)
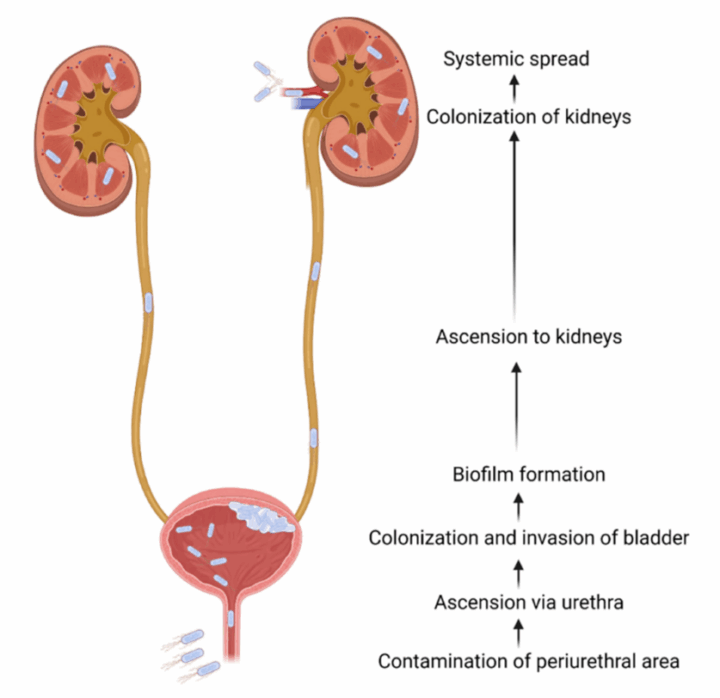
Imagen 3: Representación gráfica de la progresión de una infección bacteriana desde la vejiga hasta los riñones.
Especial atención al arándano rojo americano (Vaccinium macrocarpon), uno de los fitocompuestos mejor documentados para la prevención de la cistitis recurrente. Sus proantocianidinas tipo A inhiben la adhesión de cepas uropatógenas de Escherichia coli al epitelio vesical, reduciendo significativamente la colonización y el riesgo de infección ascendente. [1,27, 28] Diversos metaanálisis y revisiones sistemáticas han confirmado su utilidad profiláctica, con reducciones de hasta un 30–40 % en las tasas de recurrencia de ITU en mujeres, especialmente en aquellas con infecciones no complicadas. [26-28]
Si bien su efecto directo sobre el edema es nulo, su capacidad para prevenir infecciones urinarias, reducir la inflamación local y mantener la integridad del tracto urinario inferior contribuye indirectamente al éxito de estrategias terapéuticas orientadas al drenaje fisiológico y la depuración general. [1,3,24]
Desde una perspectiva integradora, también cabe mencionar la acción indirecta de compuestos como la clorofila, presente en ciertas formulaciones depurativas, por su capacidad para modular la microbiota intestinal, reducir la carga de toxinas endógenas y favorecer la función hepática, lo cual optimiza el eje hepatorrenal implicado en la homeostasis del volumen extracelular. [5,24]
Así, los agentes drenantes y preventivos urinarios no sólo potencian la diuresis sin inducir depleción hidroelectrolítica, sino que además protegen frente a infecciones urinarias bajas, especialmente en pacientes con menor volumen de diuresis, alteraciones del vaciamiento vesical o inmunocompromiso leve. [28,29] Su incorporación a esquemas terapéuticos orientados al tratamiento del edema representa una estrategia complementaria con valor clínico tangible, particularmente en mujeres jóvenes, pacientes polimedicados, personas mayores y situaciones predisponentes como el edema postural, el edema premenstrual o el posquirúrgico leve. [30,31]
En conjunto, la evidencia disponible apoya el uso de una selección de agentes vegetales con acción diurética ligera, antiséptica urinaria y depurativa sistémica, como parte de una estrategia terapéutica global en el manejo del edema no complicado, con excelente tolerabilidad y sin riesgo de efectos adversos mayores. [28,29,31]
Discusión general
El abordaje terapéutico del edema, especialmente en sus formas funcionales, causadas por las altas temperaturas o de curso leve a moderado, requiere una visión integradora que supere el modelo tradicional centrado exclusivamente en la inducción de diuresis agresiva. La fisiopatología del edema es multifactorial, e involucra interacciones entre el sistema cardiovascular, renal, hepático y linfático, así como alteraciones en la regulación neurohormonal y del volumen extracelular. [5,18,22] En este escenario, la fitoterapia, basada en el uso de extractos estandarizados con evidencia preclínica y clínica, se consolida como una herramienta complementaria cada vez más validada, tanto por su eficacia como por su perfil de tolerancia. [7,24]
La presente revisión ha sintetizado el respaldo científico disponible para distintos fitocomponentes con actividad antiedematosa, agrupados por mecanismo de acción predominante. En primer lugar, destacan las especies con efecto diurético tubular directo, como Equisetum arvense y Petroselinum crispum, cuyas acciones se han descrito tanto en estudios animales como en ensayos clínicos controlados. [6,7] Su capacidad para incrementar la excreción de agua y sodio sin comprometer la kaliemia ni activar mecanismos compensatorios excesivos representa una ventaja clara frente a los diuréticos sintéticos convencionales, especialmente en pacientes sin patología orgánica mayor. [6,7,23]
En segundo lugar, la presencia de cofactores iónicos, como el potasio, adquiere una importancia crítica desde el punto de vista clínico. La inclusión de dos formas biodisponibles de potasio, gluconato y citrato permite no sólo contrarrestar la eventual pérdida de este catión inducida por la diuresis, sino también ejercer un efecto inhibidor fisiológico sobre la secreción de aldosterona. [17,18] Este mecanismo, ampliamente descrito en fisiología endocrina, evita la activación excesiva del sistema RAAS, contribuyendo a una diuresis más estable y sostenida. Además, el citrato potásico actúa como alcalinizante urinario, lo cual puede potenciar los efectos de otros fitocomponentes con actividad uropática, como Arctostaphylos uva-ursi o Agathosma betulina. [24]
Los agentes con acción antiinflamatoria y estabilizadora de la permeabilidad capilar, como Filipendula ulmaria, Crataegus monogyna o Camellia sinensis, aportan un mecanismo complementario crucial en edemas donde existe disfunción microvascular o un componente inflamatorio de bajo grado. [11,19-21] Estos extractos, ricos en flavonoides, salicilatos y catequinas, han demostrado reducir la extravasación plasmática, proteger la integridad endotelial y mejorar el retorno venoso en modelos experimentales y observacionales. [1,10,13]
Asimismo, los drenantes fisiológicos como Zea mays y las plantas con acción uropatógena preventiva como Vaccinium macrocarpon aportan valor añadido en el manejo de pacientes con bajo volumen de diuresis, tendencia a estasis vesical o riesgo elevado de infecciones urinarias recurrentes. [1,23,25] La actividad antiadhesiva de las proantocianidinas tipo A del arándano rojo americano ha sido confirmada en metaanálisis recientes, y su inclusión en esquemas antiedematosos se justifica plenamente en pacientes seleccionados. [2,3,27](Imagen 4)
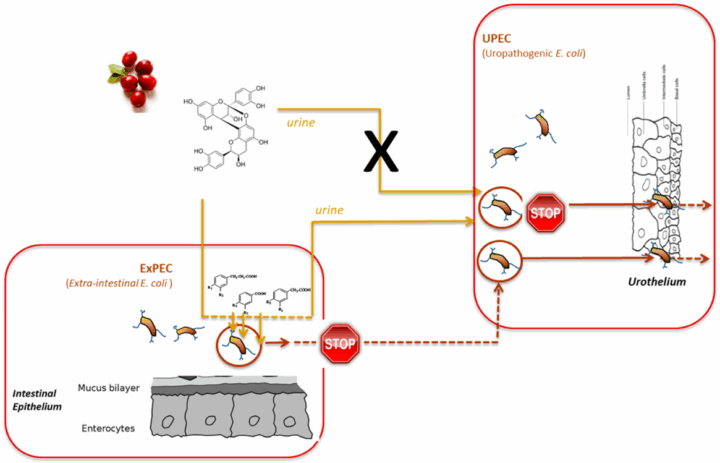
Imagen 4: Las proantocianidinas del arándano inhiben la adhesión de E. coli uropatógena (UPEC) y extraintestinal (ExPEC) al epitelio intestinal y urotelial, previniendo su colonización e infección. (32)
Todo este conjunto de mecanismos: diurético, antiinflamatorio, venotónico, inmunomodulador, detoxificante y antiséptico urinario, converge en una estrategia terapéutica integradora, más fisiológica, menos invasiva, y especialmente indicada en contextos donde el tratamiento convencional pueda resultar excesivo o mal tolerado. [5,7,22]
Actualmente, ciertas combinaciones fitoterapéuticas disponibles reúnen este perfil multimodal, integrando extractos como los aquí revisados, junto con cofactores críticos como el potasio en forma de gluconato y citrato, permitiendo así una intervención coherente con la fisiopatología del edema, y alineada con las exigencias de seguridad, eficacia y sostenibilidad clínica. [17,18,24]
Conclusiones
La evidencia científica revisada en artículo respalda de forma solida el uso racional de fitoterapia en el abordaje clínico del edema, particularmente en sus formas funcionales, idiopáticas, hormonales, posturales, vasculares leves o inducidas por condiciones ambientales como las altas temperaturas. En este contexto, la vasodilatación térmica y la reducción del tono venoso contribuyen a la extravasación de líquido hacia el intersticio, con predominio en extremidades inferiores, especialmente en pacientes predispuestos. Frente a las limitaciones del tratamiento convencional, como la depleción electrolítica, la activación neurohormonal secundaria o la intolerancia a largo plazo, y considerando que el uso prolongado de diuréticos sintéticos puede agravar la disfunción iónica y comprometer la estabilidad hemodinámica en pacientes sin patología estructural, se consolida el interés clínico por estrategias más fisiológicas, integradoras y sostenibles.
Desde esta perspectiva, Depurdren representa una aplicación terapéutica basada en evidencia, que integra en una sola formulación extractos vegetales estandarizados con acción diurética, venotónica, antiinflamatoria, drenante y antiséptica urinaria, junto con cofactores iónicos clave como el potasio en forma de citrato y gluconato. Esta combinación permite abordar el edema desde múltiples ejes fisiopatológicos, sin inducir deshidratación ni comprometer la homeostasis electrolítica, posicionándose, así como una herramienta de primera línea en el manejo de la retención de líquidos.
Referencias Bibliográficas
- Howell AB, Reed JD, Krueger CG, et al. Bioactive compounds in cranberries and their role in prevention of urinary tract infections. Mol Nutr Food Res. 2007;51(6):1023‑9.
- Luís Domingues F, Pereira L. Cranberries: systematic review & meta‑analysis of RCTs for UTI prevention. J Urol. 2017;197(3):P Mid; trial sequential analysis.
- Salo J, et al. High‑dose proanthocyanidin standardized cranberry extract for prevention of recurrent UTIs: double‑blind RCT. BMC Urol. 2021;21:44.
- Clinical trial registry NCT… potassium citrate vs chloride; increased kaliuresis & intracellular uptake. J Am Soc Nephrol. 2023;14‑.
- Dreier R, et al. Potassium citrate raises intracellular uptake and kaliuresis vs chloride. CJASN. 2023;18(8):120.
- Kreydiyyeh SI, Usta J. Inhibition of Na⁺/K⁺‑ATPase by Petroselinum crispum: natriuretic effects in rats. J Ethnopharmacol. 2002;79(3):353‑7.
- Alberti A, et al. Diuretic effect of parsley extract in human volunteers. Phytomedicine. 2020;67:153178.
- De Backer D, et al. Effects of Urtica dioica on microcirculation in CAD patients. Microcirculation. 2021;28(5):e12670.
- Grassi D, et al. Flavonoid intake and microvascular function: role of Crataegus monogyna. Nutr Rev. 2019;77(8):540‑58.
- Xu L, et al. EGCG inhibits TNF‑α induced MCP‑1 in vascular endothelia. J Neuroinflammation. 2012;9:161.
- Aldosterone Function & Production. GeeksforGeeks [Internet]. Última actualización 13 Ene 2024. Disponible en: https://www.geeksforgeeks.org/biology/aldosterone-function-production/
- Alonso‑Moran ER, et al. Potassium citrate vs chloride: modulation of aldosterone–trans tubular gradient. Clin J Am Soc Nephrol. 2023;18(6):160.
- Stokol Sodium and potassium transport in principal cells. eClinpath [Internet]. 7 Mar 202, Disponible en: https://eclinpath.com/chemistry/kidney/physiology/print-25/
- Kloska SV, et al. Venotonic mechanism of Crataegus monogyna extract WS®1442 on endothelial barrier. J Mol Cell Cardiol. 2012;52(5):101‑10.
- EMA/HMPC. Crataegus spp. monograph: herbal medicines. EMA; 2014.
- Birukova AA, et al. WS®1442 protects against endothelial hyperpermeability via cAMP/Rap1 pathway. Exp Cell Res. 2007;313(11):2504‑20.
- Marek‑Józwik B, et al. EGCG attenuates vascular dysfunction via antioxidant pathways. Sci Rep. 2022;12:21107.
- Dong XW, et al. EGCG protects endothelial cells by autophagy PI3K‑Akt‑mTOR pathway. Oxid Med Cell Longev. 2020;2020:7154459.
- Tan HY, et al. EGCG modulates senescent endothelial cell secretome. Front Cardiovasc Med. 2024;11:1506360.
- Chen Q, et al. EGCG improves endothelial function and reduces BP in hypertensive rats. AJP Endocrinol Metab. 2006;291:E36‑44.
- Jang Y, et al. Endothelial protective effect of EGCG under hyperglycemic stress. J Mol Cell Cardiol. 2013;60:C5‑11.
- Zhang C, et al. EGCG improves NO bioavailability via eNOS coupling. Nitric Oxide. 2022;105:1‑9.
- Phatak A, et al. Potassium homeostasis: physiology and pharmacotherapy. Pharmacol Rev. 2023;75(3):328‑59.
- Bruni R, et al. Arbutin derivatives from Arctostaphylos uva‑ursi: antimicrobial & diuretic effects. Phytomedicine. 2022;93:153742.
- McKay DL, Blumberg JB. Role of tea catechins in vascular health: EGCG perspective. Pharmacol Res. 2007;55(3):208‑19.
- Dickson K, Zhou J, Lehmann C. Lower urinary tract inflammation and infection: Key microbiological and immunological aspects. J Clin Med. 2024;13(2):315. Available from: https://doi.org/10.3390/jcm13020315
- Velázquez‑Durán LM, et al. Zea mays extract: diuretic effect in rodents & electrolyte balance. J Ethnopharmacol. 2019;236:204‑12.
- Juturu V, Zakarian F, et al. Vaccinium macrocarpon supplement reduces UTI recurrence: meta‑analysis of 23 RCTs. PLoS ONE. 2021;16(9):e0257483.
- Liu J, et al. Cranberry products for UTI prevention: 7 RCT meta‑analysis. Am J Clin Nutr. 2017;106(2):496‑501.
- Wang CH, et al. Cranberry juice vs tablets: impact on UTI prevention in women. J Urol. 2022;207(6):1222‑30.
- Månsson LE, et al. Whole cranberry powder reduces UTI incidence in adults: RCT. Br J Nutr. 2025;133(4):521‑9.
- Konesan J, Liu L, Mansfield KJ. The Clinical Trial Outcomes of Cranberry, D‑Mannose and NSAIDs in the Prevention or Management of Uncomplicated Urinary Tract Infections in Women: A Systematic Review. Pathogens. 2022;11(11):1471. doi:10.3390/pathogens11111471
