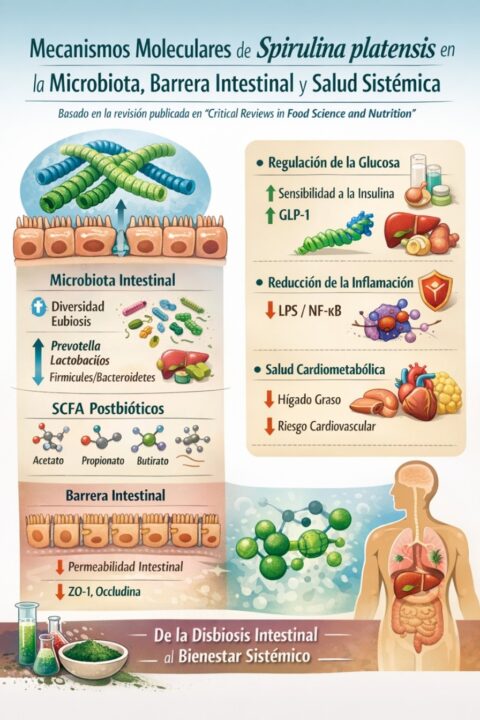
Resistencia a la Insulina: El Eje Metabólico Oculto de la Patología Moderna
15 de abril de 2026
Nota editorial: Este artículo constituye una revisión, análisis y puesta al día clínica del trabajo “Shedding light on the impacts of Spirulina platensis on gut microbiota and related health benefits”, publicado en la revista Critical Reviews in Food Science and Nutrition.
Por qué esta revisión redefine el potencial clínico de la Spirulina
La Spirulina (taxonómicamente, Arthrospira platensis) ha trascendido su etiqueta popular de “superalimento” para consolidarse como matriz nutracéutica pleiotrópica: rica en proteínas, pigmentos funcionales y compuestos bioactivos con capacidad de modular múltiples ejes fisiológicos.
El giro de enfoque que propone la revisión no es tanto “si puede aportar beneficios”, sino cómo: situando el eje microbiota–barrera intestinal–metabolitos como una plataforma mecanística capaz de influir en inflamación de bajo grado, estrés oxidativo y metabolismo glucolipídico. En otras palabras: Spirulina no actúa únicamente “por lo que contiene”, sino por cómo reordena la ecología intestinal y cómo esa reprogramación se traduce en señales sistémicas.
1. El Core Mecanístico: De la Disbiosis a la Señalización Metabólica
La revisión se apoya en una bisagra fisiopatológica clave de la clínica moderna: disbiosis + pérdida de función de barrera (“leaky gut”) + inflamación crónica de bajo grado (metaflamación).
En Salud de Precisión, esta lógica es especialmente útil porque conecta piezas que en consulta aparecen separadas: exceso de adiposidad, disglucemias, dislipidemia, hipertensión, hígado graso y síntomas “inflamatorios” inespecíficos. El intestino funciona como órgano sensorial y endocrino: si la barrera se debilita, aumenta el paso de señales proinflamatorias (como LPS) y se amplifica la activación inmune-metabólica (p. ej., TLR4/MyD88/NF-κB), con impacto sobre endotelio, hígado y tejido adiposo.
2. Hallazgos Clave en la Composición de la Microbiota Intestinal
La revisión integra evidencia de modelos animales y estudios clínicos y describe un patrón global asociado a la suplementación con S. platensis: aumento de diversidad y cambios composicionales con relevancia metabólica.
A) Restauración de la Diversidad y Resiliencia
Se reporta un aumento de la alfa-diversidad. Clínicamente, una microbiota más diversa suele interpretarse como un ecosistema con mayor “resiliencia funcional”: mejor capacidad de amortiguar perturbaciones (dieta, fármacos, estrés), favorecer resistencia a colonización por oportunistas y mantener producción de metabolitos beneficiosos.
B) Reprogramación del Perfil Filogenético y Funcional
La revisión destaca, de forma repetida en distintos modelos:
- Reducción del cociente Firmicutes/Bacteroidetes (F/B).
- Aumento relativo de Prevotella.
- Enriquecimiento de Lactobacillaceae.
Desde una lectura funcional, este patrón suele alinearse con una microbiota con mayor capacidad fermentativa de sustratos dietéticos y mejor “tono metabólico” (más producción de SCFA, menos señales proinflamatorias, mejor perfil de permeabilidad). La revisión, además, conecta estos cambios con desenlaces clínicos “macro” (antiobesidad, antidiabético, antihipertensivo, hipolipemiante, antiinflamatorio y antioxidante).
3. La Vía de los Postbióticos: Ácidos Grasos de Cadena Corta (SCFA) y Butirato
Este es uno de los núcleos mecanísticos más atractivos para el clínico: la revisión describe que S. platensis se asocia con un aumento de la producción de SCFA.
¿Por qué importa? Porque los SCFA (acetato, propionato y butirato) no son solo “subproductos”:
- Nutren al epitelio (especialmente el butirato para colonocitos), favoreciendo integridad y reparación.
- Funcionan como moléculas señalizadoras que modulan inflamación y metabolismo (vía receptores y rutas intracelulares).
- Se relacionan con regulación de hormonas intestinales implicadas en saciedad y homeostasis glucémica (p. ej., señalización tipo GLP-1/PYY), un puente directo entre microbiota y fenotipo cardiometabólico.
De forma coherente con este marco, un estudio centrado en ficocianina (componente característico de Arthrospira) mostró incremento de diversidad, aumento de familias bacterianas con potencial butirato-productor (p. ej., Lachnospiraceae y Ruminococcaceae) y reducción de permeabilidad intestinal junto con menor señal de endotoxemia (LPS).
4. Refuerzo de la Barrera Intestinal: Un Pilar Antiinflamatorio
La revisión reporta un hallazgo clínicamente decisivo: la suplementación con S. platensis se asocia con disminución de la permeabilidad intestinal.
A nivel molecular, esto se entiende como un refuerzo de la arquitectura de uniones estrechas (tight junctions), con proteínas como ZO-1, occludina y claudinas funcionando como “remaches” que mantienen la selectividad del epitelio.
Un modelo animal muy citado en este campo (ratas con dieta alta en grasa) mostró que S. platensis:
- Reduce el aumento de permeabilidad (medida por FITC-dextran).
- Recupera proteínas de tight junction (ZO-1 y occludina).
- Disminuye la activación TLR4/MyD88/NF-κB (p65), un eje clásico de inflamación inducida por endotoxemia metabólica.
Esto tiene traducción clínica directa: menos permeabilidad suele significar menor translocación de estímulos proinflamatorios, menor “ruido inmunitario” sistémico y, por tanto, un terreno más favorable para modular resistencia a insulina, disfunción endotelial y riesgo cardiometabólico en fenotipos sensibles.
En humanos, además, un ensayo doble ciego en pacientes con SII-C (IBS-C) observó una reducción del marcador de permeabilidad zonulina tras suplementación con Spirulina, apuntando a que este eje barrera-inflamación también puede ser clínicamente modulable.
5. Complejo Bioactivo: Más allá de una Matriz Nutricional
La revisión sugiere que el efecto de S. platensis no se explica por un único compuesto, sino por una sinergia de elementos bioactivos.
Como lectura mecanística útil para el profesional, tres candidatos destacan por su plausibilidad y coherencia con el eje intestino-sistema:
- C-Ficocianina
Más que pigmento antioxidante: la evidencia experimental sugiere que puede reconfigurar microbiota, favorecer bacterias funcionales y mejorar barrera (incluida reducción de LPS).
- Polisacáridos complejos
Funcionan como sustratos fermentables con potencial prebiótico, facilitando producción de SCFA y el perfil eubiótico descrito en la revisión.
- Péptidos bioactivos
Derivados proteicos con posible papel en tono inflamatorio, señal vascular y, en algunos modelos, control de presión arterial y metabolismo.
En conjunto, este “complejo bioactivo” encaja con la idea de intervención sobre el terreno: no reemplaza dieta, sueño, ejercicio ni control de factores de riesgo, pero puede actuar como palanca sobre inflamación, oxidación y función de barrera en pacientes seleccionados.
6. Integración en la Práctica Clínica de Precisión
Sin caer en reduccionismos, esta revisión aporta base para considerar S. platensis dentro de una estrategia multimodal en fenotipos concretos, especialmente donde el eje intestino-metabolismo está “encendido”: síndrome metabólico, exceso de adiposidad con inflamación de bajo grado, disglucemias y dislipidemias con componente inflamatorio.
Biomarcadores para la monitorización clínica
El seguimiento debería ser congruente con el objetivo terapéutico:
- Metabólicos/Hormonales: glucosa basal, insulina basal (HOMA-IR cuando proceda), HbA1c.
- Lipídicos: TG, LDL-C, HDL-C; y, si se trabaja con riesgo avanzado, ApoB.
- Inflamatorios/Oxidativos: PCR-us como eje práctico.
Aquí es interesante una pieza complementaria: una revisión sistemática y metaanálisis reciente encontró que la suplementación con Spirulina se asoció a una reducción significativa de PCR (WMD ≈ −0,55 mg/L), lo que es coherente con la hipótesis antiinflamatoria propuesta por la revisión central y con el concepto de “metaflamación” como motor cardiometabólico.
7. El Factor Crítico: Seguridad, Calidad y Trazabilidad
Este punto es innegociable, especialmente en un producto de origen biológico cuya composición final depende de agua, cultivo, cosecha y procesado.
Autoridades sanitarias europeas han señalado que los suplementos con spirulina pueden contaminarse con cianotoxinas (microcistinas), bacterias o metales pesados y recomiendan priorizar canales y fabricantes con trazabilidad y controles.
En la misma línea, la FDA describe investigaciones y vigilancia sobre microcistinas en suplementos de algas verde-azuladas, con hallazgos variables según producto y lotes.
Y estudios analíticos de mercado han detectado microcistinas en productos comerciales de spirulina, con niveles que, según dosis de consumo, podrían acercar o superar límites recomendados.
Traducción clínica (práctica y directa):
- Priorizar terceros análisis, GMP/controles de contaminantes y trazabilidad.
- Recordatorio útil: agencias como ANSES también subrayan matices prácticos (p. ej., no considerarla fuente fiable de B12 para veganos, y precauciones en predisposición alérgica o fenilcetonuria).
Conclusión y Perspectiva
La revisión publicada en Critical Reviews in Food Science and Nutrition dota a Spirulina platensis de un marco mecanístico robusto y alineado con la Salud de Precisión: modulación de microbiota, aumento de postbióticos (SCFA) y refuerzo de la barrera intestinal, con asociación a beneficios sistémicos (metabólicos, inflamatorios y cardiovasculares).
El mensaje clave para el clínico es claro: existe una hipótesis terapéutica nutracéutica con plausibilidad biológica. Su rendimiento real dependerá de (1) fenotipación correcta, (2) integración en un plan multimodal (nutrición, ejercicio, sueño, control de riesgo), y (3) una exigencia estricta de calidad, seguridad y trazabilidad del producto.
Bibliografía
Alves, J. L. de B., Costa, P. C. T. da, Sales, L. C. S., Luis, C. C. S., Bezerra, T. P. T., Souza, M. L. A., Costa, B. A., & de Souza, E. L. (2025). Shedding light on the impacts of Spirulina platensis on gut microbiota and related health benefits. Critical Reviews in Food Science and Nutrition, 65(11), 2062–2075. https://doi.org/10.1080/10408398.2024.2323112
ANSES. (n.d.). Food supplements containing spirulina: the importance of choosing trustworthy supply channels. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail.
Food and Drug Administration. (2024). Blue-Green Algae Products and Microcystins.
Jazinaki, M. S., et al. (2025). Effects of Spirulina Supplementation on C-Reactive Protein (CRP): A Systematic Review and Dose–Response Meta-Analysis.
Nasab, S. J., et al. (2025). Effects of Spirulina (Arthrospira) platensis supplementation on intestinal permeability, oxidative stress markers, quality of life, and disease severity in patients with constipation-predominant irritable bowel syndrome: A randomized double-blind, placebo-controlled trial.
Rhoades, J., et al. (2023). Microbiota and Cyanotoxin Content of Retail Spirulina Supplements and Spirulina Supplemented Foods.
Xie, Y., et al. (2019). Effects of phycocyanin in modulating the intestinal microbiota of mice.
Yu, T., et al. (2020). Spirulina platensis alleviates chronic inflammation with modulation of gut microbiota and intestinal permeability in rats fed a high-fat diet.
