
Decisiones en la transición menopáusica: cómo moldear el futuro biológico de la mujer
1 de abril de 2026
Introducción: ¿y si el sistema inmune no fuera solo defensa, sino metabolismo en acción?
Durante décadas, la inmunología se enseñó como un sistema binario: se activa frente a una amenaza y se apaga cuando esta desaparece. Una visión elegante, pero incompleta.
Hoy sabemos que la pregunta esencial no es únicamente qué activa a una célula inmunitaria, sino algo más profundo:
¿de dónde obtiene la energía para hacerlo y qué ocurre cuando esa maquinaria metabólica pierde coherencia?
El sistema inmune no responde solo a señales químicas. Responde a decisiones energéticas. Cada vez que un linfocito se activa, cambia su programa metabólico. Cada vez que un macrófago se polariza, reorganiza su arquitectura mitocondrial. Cada vez que una célula NK aumenta su citotoxicidad, incrementa su demanda bioenergética.
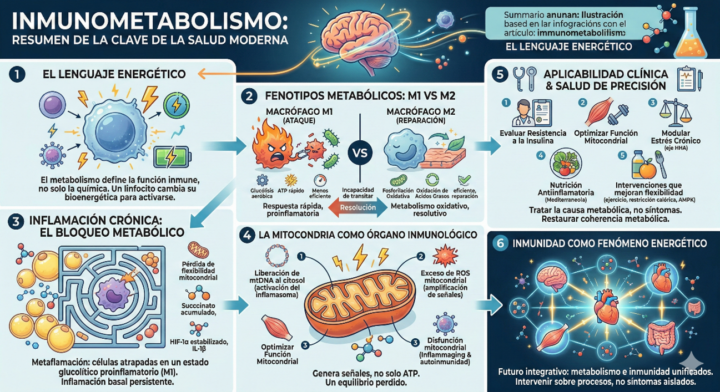
El inmunometabolismo no es un fenómeno accesorio. Es el núcleo operativo de la respuesta inmune.
Y comprenderlo transforma la forma en que interpretamos inflamación crónica, autoinmunidad, síndrome metabólico, dolor persistente y envejecimiento biológico.
Cuando la energía decide el destino inmunológico
En estado basal, una célula inmunitaria es eficiente y discreta. Utiliza principalmente fosforilación oxidativa (OXPHOS), una vía que maximiza la producción de ATP por molécula de sustrato.
Pero cuando detecta una señal de peligro, la eficiencia deja de ser prioritaria. Lo que importa es la velocidad.
Se produce entonces un cambio hacia la glucólisis aeróbica —un fenómeno metabólicamente similar al efecto Warburg descrito en oncología—. Aunque menos eficiente en términos de ATP, esta vía permite generar intermediarios biosintéticos necesarios para proliferación y producción de citocinas.
Este cambio no es consecuencia secundaria de la activación. Es parte estructural de ella.
En macrófagos, la polarización clásica M1 depende de glucólisis intensificada y un ciclo de Krebs “interrumpido”, con acumulación de metabolitos como succinato. Por el contrario, los macrófagos con perfil regulador o resolutivo (M2) mantienen integridad del ciclo de Krebs y dependen más de OXPHOS y oxidación de ácidos grasos.
En linfocitos T ocurre algo similar. Las células T naïve utilizan metabolismo oxidativo. Al activarse, migran hacia glucólisis. En cambio, las células T reguladoras y las células T memoria vuelven a depender en mayor medida de metabolismo mitocondrial eficiente.
La clave clínica es clara: si una célula pierde su capacidad de transición entre estos estados —es decir, si pierde flexibilidad metabólica—, queda atrapada funcionalmente.
Y la inflamación deja de ser resolutiva para volverse persistente.
Inflamación crónica: cuando la célula queda metabólicamente bloqueada
En obesidad, resistencia a la insulina o estrés crónico sostenido, las células inmunes no solo se activan; quedan reprogramadas.
El tejido adiposo expandido no es metabólicamente neutro. Libera ácidos grasos libres, señales inflamatorias y DAMPs que activan macrófagos residentes. Estos adoptan un perfil proinflamatorio mantenido, dependiente de glucólisis.
Uno de los metabolitos más estudiados en este contexto es el succinato. Su acumulación estabiliza HIF-1α, promoviendo transcripción de IL-1β y perpetuando inflamación. No estamos ante un simple exceso de citocinas; estamos ante un circuito metabólico autorreforzado.
Este fenómeno ha sido descrito como “metaflamación”: inflamación inducida por exceso nutricional y desregulación metabólica, no por infección.
El sistema inmune deja de reaccionar ante un patógeno y comienza a reaccionar ante el entorno metabólico.
La pregunta clínica entonces cambia:
¿qué señal metabólica está manteniendo esta inflamación activa?
La mitocondria como órgano inmunológico
Durante años enseñamos que la mitocondria era la “central energética” de la célula. Hoy sabemos que es también un nodo central de señalización inmunológica.
La liberación de ADN mitocondrial al citosol puede activar receptores intracelulares que reconocen patrones moleculares de peligro. El ADN mitocondrial, por su origen bacteriano evolutivo, es interpretado como una señal de amenaza.
Además, la producción excesiva de ROS mitocondriales no es simplemente daño colateral. En niveles controlados, actúa como señal reguladora. Pero cuando se desborda, amplifica cascadas inflamatorias.
En envejecimiento, la acumulación de mitocondrias disfuncionales contribuye a un estado inflamatorio crónico de bajo grado, fenómeno conocido como inflammaging. Las células inmunes envejecidas muestran menor capacidad bioenergética, menor eficiencia mitocondrial y mayor tendencia a producir citocinas proinflamatorias.
La mitocondria no solo produce ATP. Produce contexto inmunológico.
Inmunometabolismo y enfermedades modernas
Lo fascinante del inmunometabolismo es que conecta procesos aparentemente dispares.
Un paciente con resistencia a la insulina no presenta únicamente alteración glucémica. Presenta activación inmunometabólica persistente.
Una mujer con dolor crónico puede mostrar microglía metabólicamente activada en el sistema nervioso central.
Un adulto mayor frágil puede tener linfocitos incapaces de sostener un programa metabólico eficaz frente a una vacuna.
En enfermedades autoinmunes, la reprogramación metabólica de linfocitos T favorece expansión de subpoblaciones inflamatorias. En cáncer, el microambiente tumoral altera el metabolismo de células T infiltrantes, limitando su eficacia.
El metabolismo se convierte en el terreno común.
Aplicabilidad clínica: de la PCR al contexto metabólico
La práctica clínica tradicional mide inflamación a través de marcadores como PCR o VSG. Son útiles, pero insuficientes.
La pregunta relevante es:
¿Qué está sosteniendo metabólicamente esa inflamación?
Desde una perspectiva de Salud de Precisión, esto implica evaluar resistencia a la insulina incluso en pacientes con glucemias normales. Implica valorar composición corporal y masa muscular como determinantes inmunológicos. Implica entender el impacto del estrés crónico sobre el eje HHA y su influencia metabólica.
El ejercicio físico no solo mejora capacidad cardiovascular; reprograma inmunometabolismo. Activa AMPK, estimula biogénesis mitocondrial, favorece transición hacia perfiles inmunitarios más reguladores.
La restricción calórica controlada y el ayuno intermitente pueden inducir mejoras en eficiencia mitocondrial y reducir inflamación basal en determinados contextos.
La nutrición mediterránea, rica en polifenoles y ácidos grasos monoinsaturados, modula rutas inflamatorias y mejora perfil metabólico sistémico.
No estamos “subiendo defensas”. Estamos restaurando coherencia energética.
El sistema inmune como red energética dinámica
El sistema inmune no es un interruptor. Es una red que traduce señales metabólicas en decisiones funcionales.
Cuando la energía fluye de forma flexible, la respuesta es proporcional y resolutiva.
Cuando la energía se distorsiona, la inflamación se cronifica.
La medicina moderna ha avanzado enormemente en terapias biológicas dirigidas a citocinas específicas. Pero si no abordamos el sustrato metabólico, muchas intervenciones quedan incompletas.
El metabolismo no acompaña a la inmunidad. La estructura.
Conclusión: la integración como paradigma clínico
El inmunometabolismo nos obliga a abandonar compartimentos estancos entre endocrinología, inmunología y metabolismo.
La inflamación crónica, el envejecimiento acelerado y muchas enfermedades modernas comparten una raíz bioenergética común.
Al integrar metabolismo e inmunidad, pasamos de tratar manifestaciones a intervenir sobre procesos.
El futuro clínico no reside en separar sistemas.
Reside en entender su interdependencia energética.
Y en esa comprensión, el inmunometabolismo se convierte en uno de los pilares más prometedores de la práctica médica contemporánea.
Bibliografía
-
- O’Neill, L. A. J., Kishton, R. J., & Rathmell, J. (2016). A guide to immunometabolism for immunologists. Nature Reviews Immunology, 16, 553–565.
https://www.nature.com/articles/nri.2016.70 - Buck, M. D., Sowell, R. T., Kaech, S. M., & Pearce, E. L. (2017). Metabolic instruction of immunity. Cell, 169(4), 570–586.
https://www.cell.com/cell/fulltext/S0092-8674(17)30413-9 - Pearce, E. L., & Pearce, E. J. (2013). Metabolic pathways in immune cell activation and quiescence. Science, 342(6157), 1242454.
https://www.science.org/doi/10.1126/science.1242454 - Mills, E. L., & O’Neill, L. A. J. (2016). Reprogramming mitochondrial metabolism in macrophages. Nature Reviews Immunology, 16, 437–446.
https://www.nature.com/articles/nri.2016.84 - Hotamisligil, G. S. (2017). Inflammation, metaflammation and immunometabolism. Nature, 542, 177–185.
https://www.nature.com/articles/nature21363 - López-Otín, C., Blasco, M. A., Partridge, L., Serrano, M., & Kroemer, G. (2023). Hallmarks of aging: An expanding universe. Cell, 186(2), 243–278.
https://www.cell.com/cell/fulltext/S0092-8674(22)01570-7 - Ganeshan, K., & Chawla, A. (2014). Metabolic regulation of immune responses. Annual Review of Immunology, 32, 609–634.
https://www.annualreviews.org/doi/10.1146/annurev-immunol-032713-120236 - Diskin, C., & Pålsson-McDermott, E. M. (2018). Metabolic modulation in macrophage effector function. Frontiers in Immunology, 9, 270.
https://www.frontiersin.org/articles/10.3389/fimmu.2018.00270 - Phan, A. T., Goldrath, A. W., & Glass, C. K. (2017). Metabolic and epigenetic coordination of T cell and macrophage immunity. Immunity, 46(5), 714–729.
https://www.cell.com/immunity/fulltext/S1074-7613(17)30218-9 - Boussiotis, V. A. (2022). Molecular and biochemical aspects of the PD-1 checkpoint pathway. New England Journal of Medicine, 386, 1767–1778.
(Conexión inmunometabolismo–microambiente tumoral)
- O’Neill, L. A. J., Kishton, R. J., & Rathmell, J. (2016). A guide to immunometabolism for immunologists. Nature Reviews Immunology, 16, 553–565.
